Unser Puffersystem und Baustein für Wachstum
Hey liebe Freunde der Meerwasser-Aquaristik und ein freundliches „Ciao“ aus dem Süden Italiens. Ich befinde mich aktuell in Elternzeit und wir nutzen die gemeinsame Zeit für eine tolle Reise in den begehrten Süden Italiens – genauer auf die Insel Sardinien. Selbst hier unter schönen Pinien direkt neben einem wundervoll weißen Puderzuckerstrand mit türkisem Wasser, lass ich es mir nicht nehmen, weiter an unserer Blogserie „Pro-Series“ zu schreiben 😊.
Wie in unserem ersten Artikel erwähnt, folgt an dieser Stelle der Artikel zum Thema „Alkalinität“. Viele wissen zwar wovon wir im Grunde sprechen, allerdings wissen wenige, worum es sich tatsächlich im Detail handelt und wie viel Potenzial wir an dieser Stelle noch herausholen können.
Die Alkalinität oder auch „Karbonathärte“ steht in einem direkten Zusammenhang mit dem pH-Wert und deshalb habe ich mich dazu entschieden, diesen Artikel direkt nach dem „pH-Wert“ Blogbeitrag zu verfassen.
Solltest du unsere Blogbeiträge spannend und interessant finden, so freuen wir uns sehr über einen Kommentar am Ende des Artikels.
Was ist die Alkalinität?
Erklärung und Definition
 KH in Pulverform
KH in Pulverform
Die Alkalinität oder auch Karbonathärte gibt an, wie viel Säure – in unserem speziellen Fall CO2 (Kohlenstoffdioxid) – wir dem Wasser zugeben können, ohne dass sich der pH-Wert verändert. Es handelt demnach um ein Puffersystem – man nennt es auch Säurebindungsvermögen oder Säurebindungskapazität. Ohne ein derartiges Puffersystem würden sich die im Laufe des Tages schwankenden CO2 Konzentrationen unmittelbar auf unseren pH-Wert auswirken und unsere Pfleglinge massiv stressen.
Im Meerwasser wird die Alkalinität zu ca. 97 % durch Carbonate und Hydrogencarbonate erzeugt. Die restlichen 3 % übernehmen Borsäure, Kieselsäure, Orthophosphate und Magnesium. Wir konzentrieren uns allerdings auf die 97 % Carbonat und Hydrogencarbonat.
Die Carbonate und Hydrogencarbonate haben allerdings noch eine weitere Verwendung. Sie werden zur Kalzifizierung unter Zunahme von Calcium-Ionen (Ca2+) zu Kalziumkarbonat (CaCO3) - auch Kalk genannt - gefällt und stellen somit den Grundbaustein zum Wachsen aller kalzifizierenden Organismen. Das entzieht unserem System Carbonat bzw. Hydrogencarbonat, welches wiederum durch eine Versorgung aufgefüllt werden muss – der klassische KH-Kanister eben.
Wozu ein Puffersystem?
Ein detaillierter Blick auf das CO2
Einige werden sich jetzt vielleicht fragen, woher diese Säure kommt, die unser Puffersystem auffangen muss. An dieser Stelle möchten wir uns primär auf das Kohlenstoffdioxid (CO2) konzentrieren, da es den allergrößten Teil ausmacht.
Unsere Fische produzieren bei der Aufnahme von Sauerstoff (O2) CO2 und geben dieses an das Wasser ab. Bakterien produzieren CO2 und organische Zersetzungsprozesse erzeugen es ebenfalls. Wir haben also jede Menge CO2 Produzenten innerhalb unseres Wassers. Diese Prozesse schwanken auch innerhalb eines Tages durch bspw. die Fotosynthese.
Zusätzlich kommt noch ein weiterer Punkt hinzu: Denn auch das atmosphärische bzw. in der Umgebungsluft befindliche CO2 spielt eine große Rolle. Zwischen der CO2 Konzentration im Becken und derer in der Umgebungsluft stellt sich immer ein Gleichgewicht ein. Heißt: Ist die Konzentration in unserem Wasser niedriger als in dem Raum, in dem das Aquarium steht, wird das Wasser CO2 aufnehmen. Umgekehrt wird das Becken bei mehr CO2 im Wasser als in der Luft, das CO2 versuchen abzugeben. Dieser Vorgang findet überall dort statt, wo sich beide Medien treffen. Also an der Wasseroberfläche – je nach Oberflächenströmung - und primär dem Abschäumer.
Dieses CO2 würde jetzt unser Meerwasser saurer machen und somit den pH-Wert senken. Allerdings kommt hier unser Puffer-System - die Alkalinität - zum Tragen.
Was passiert jetzt mit dem CO2?
Gehen wir etwas tiefer in die Materie
Sobald das CO2 in unser Wasser gelangt, verbindet sich das CO2 mit dem Wasser (H2O) zu Kohlensäure (H2CO3). Im zweiten Schritt splittet sich ein Proton (H+) ab und es entsteht ein Hydrogencarbonation (HCO3-) und ein Proton (H+).
CO2 + H2O = H2CO3 = H+ + HCO3-
Ein Teil der entstandenen Hydrogencarbonat-Ionen splittet ein weiteres Proton (H+) je nach pH-Wert ab und wird zu einem Carbonation (CO32-) und einem weiteren Proton (H+).
HCO3- = H+ + CO32-
Nachdem unser pH-Wert durch die Konzentration an Protonen (H+) bestimmt wird, und wir jetzt davon mehr haben - in diesem Beispiel zwei Protonen - würde unser Wasser saurer werden. Unser pH-Wert würde sinken.
Allerdings haben wir bei einer entsprechenden Alkalinität bzw. Konzentration an Carbonaten unseres Beckens noch weitere Hydrogencarbonat-Ionen und Carbonat-Ionen im Wasser, wovon die Hydrogencarbonat-Ionen jeweils ein Proton und die Carbonat-Ionen sogar zwei Protonen aufnehmen werden, um zu Kohlensäure/Hydrogencarbonat zu reagieren. Es werden also die „freien“ Protonen (H+) reduziert und somit die Säure neutralisiert.
H+ + CO32- = HCO3- + H+ = H2CO3
Wie viele freigewordene Protonen also aufgenommen werden können oder mit anderen Worten wieviel CO2 hinzugegeben werden kann, ohne dass sich unser pH-Wert ändert, hängt vom Gehalt an Carbonaten im Wasser ab. Diese Carbonate dosieren wir über unser Versorgungssystem in Form von Natriumhydrogencarbonat (NaHCO3), um einerseits weitere Carbonate hinzuzufügen und andererseits die durch Wachstum zu Kalk ausgefällten zu ergänzen.
Kohlenstoff Gleichgewicht
Anorganische Kohlenstoffverteilung abhängig vom pH-Wert
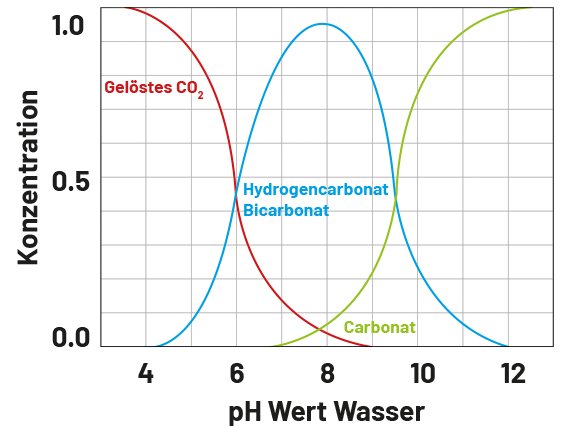 Konzentration und pH-Wert
Konzentration und pH-Wert
Abhängig vom pH-Wert und demnach abhängig von der Leistungsfähigkeit bzw. Säurebindungskapazität (Alkalinität) unseres Meerwassers entstehen durch das Kohlenstoff-Gleichgewicht jetzt unterschiedliche Konzentrationen an: Protonen (H+), Kohlensäure, Hydrogencarbonat-Ionen und Carbonat-Ionen. Die jeweiligen Verbindungen ändern sich rasend schnell und immer wieder.
Die Gleichung sieht so aus:
CO2 + H2O ↔ H2CO3 ↔ H+ + HCO3– ↔ 2 H+ + CO32–
Ein optimaler pH-Wert bedeutet also weniger Protonen (H+) im Wasser und verschiebt das Verhältnis von Carbonat-Ionen zu Hydrogencarbonat-Ionen in Richtung Carbonat-Ionen und ist somit der Alkalinität zusätzlich dienlich, denn ein Carbonation kann die doppelte Menge an Protonen aufnehmen.
Zudem ist die Kalzifizierung (Ca2+ + CO32- = CaCO3 (Calciumcarbonat / Kalk)) für unsere kalzifizierenden Organismen effizienter, da sie das überschüssige Proton aus dem Hydrogen-Carbonation nicht durch das Schleußerenzym loswerden müssen. Sie können die freigewordenen Energieressourcen also anderweitig verwenden – bspw. in Wachstum, Färbung und allgemeine Vitalität.
Eine ausreichende Säurebindungskapazität bzw. Alkalinität und demnach ein stabil optimaler pH-Wert ist also sowohl für unser Korallenwachstum als auch für die Vitalität unserer Tiere signifikant!
Wie wir die Alkalinität messen
Und was bedeutet eigentlich das Ergebnis?
 Alkalinität messen mit dem HANNA Test
Alkalinität messen mit dem HANNA Test
Wir messen direkt das Säurebindungsvermögen, indem wir unserer Meerwasser-Probe eine verdünnte Säure mit Farbindikator zugeben. Der Farbindikator wiederum schlägt um, sobald die Probe den pH-Wert der Säure und damit der initialen Farbe erreicht hat. Die verwendeten Tropfen können anschließend direkt in die Einheit °dH umgerechnet werden.
Bei anderen Testverfahren bspw. wird eine fest definierte Menge an Säure hinzugegeben und die resultierende Farbe gemessen (fotometrischer Test).
Mit anderen Worten: Umso höher der °dH Wert ist, umso mehr Säure kann hinzugegeben werden und umso stabiler ist unser System gegen pH-Schwankungen. Wir nutzen einen Wert von ca. 8-9° dH in unseren Becken, weil wir dort die Vorzüge der hohen Alkalinität haben und andererseits auch mal technische Fehler ohne größere Konsequenzen kompensiert werden können, ohne dass das die Alkalinität kritisch niedrig wird.
Kommentare werden vor der Veröffentlichung durch unsere Moderatoren geprüft und freigeschaltet.

Schon immer hat sich Tobias ein Meerwasser-Aquarium gewünscht. 2018 war es dann soweit - der erste Nanowürfel wurde angeschafft. Seitdem ist er vom Meerwasser-Virus infiziert. Aktuell pflegt er sein privates 525XL und eine weitere SPS-Zuchtanlage und lebt dieses Hobby umso intensiver.
Wir konnten leider keine Ergebnisse finden.
Möglicherweiße helfen folgende Tipps:
- Achte darauf, dass alle Wörter richtig geschrieben sind.
- Probiere es mit anderen Suchbegriffen.
- Probiere es mit allgemeineren Suchbegriffen.


